عروض باوربوينت درس قوانين سرعة التفاعل الكيميائي مادة الكيمياء 3 مقررات

عروض باوربوينت درس قوانين سرعة التفاعل الكيميائي مادة الكيمياء 3 مقررات تعتبر مؤسسة التحاضير الحديثة واحدة من أهم المؤسسات وأكثرهم شهرة داخل المملكة العربية السعودية ، ويرجع ذلك لجودة التحاضير التي تقدمها في مختلف المواد الدراسية المختلفة بداية من مرحلة رياض الأطفال والتعليم المستمر والتعليم الفكري وغيرها ، حيث تقدم تحاضير معدة بأكثر من أسلوب واستراتيجية شرح حديثة وكل هذا بأسعار تنافسية .
عروض باوربوينت درس قوانين سرعة التفاعل الكيميائي مادة الكيمياء 3 مقررات

تعمل مؤسسة التحاضير الحديثة على تطوير الملفات الخاصة بها بشكل مستمر لكي تواكب التطور الذي يحدث في المنظومة التعليمية ، حيث تقوم بتوفير مجموعة متنوعة من الشرائح التفاعلية والتي يحتاجها المعلم لكي يقوم بشرح الدروس الخاصة بالمادة بأسلوب بسيط وتفاعلي .
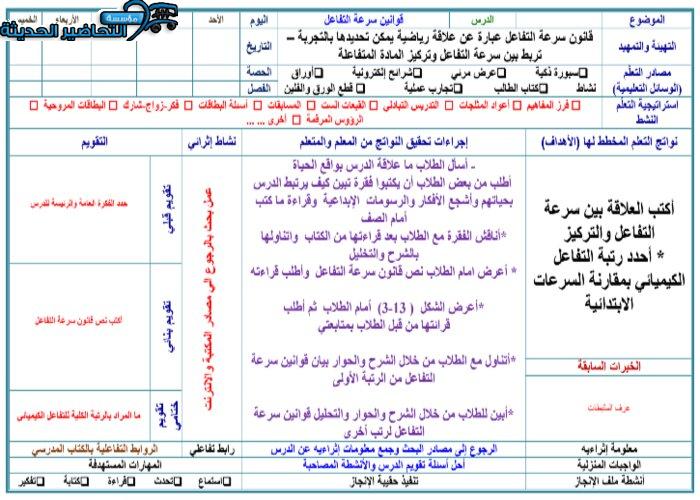
تحضير درس قوانين سرعة التفاعل الكيميائي مادة الكيمياء 3 مقررات [varnumber]
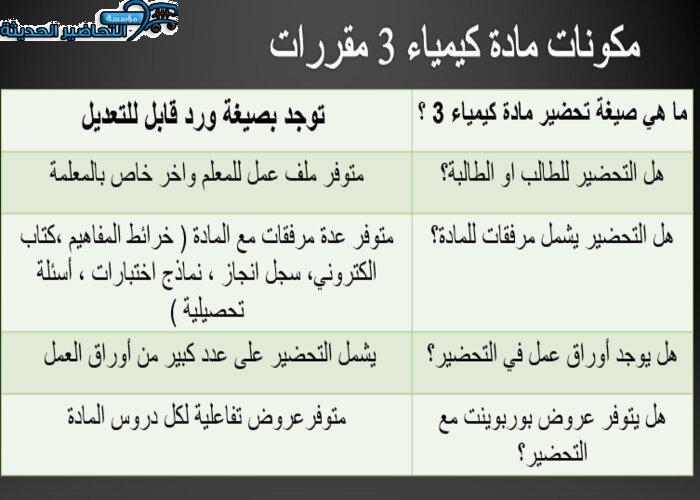
مكونات مادة الكيمياء 3 مقررات [varnumber]
طرق تحضير مادة الكيمياء 3 مقررات [varnumber]

إذا كنت ترغب في الحصول على تحضير مادة كيمياء 3 مقررات [varnumber]
لشراء تحضير مادة كيمياء 3 مقررات [varnumber]
شرح درس قوانين سرعة التفاعل الكيميائي مادة الكيمياء 3 مقررات
قانون سرعة التفاعل :
تعلمت في وقت سابق كيفية حساب متوسط معدل التفاعل الكيميائي ، كلمة “متوسط” مهمة ، نظرًا لأن معظم التفاعلات الكيميائية تتباطأ عند نفاد المواد المتفاعلة ، فإن عدد الجسيمات المتاحة للتصادم يتناقص ، وضع الكيميائيون نتائج نظرية الاصطدام في معادلة تسمى قانون معدل التفاعل ، والتي تتناول العلاقة بين معدل التفاعل الكيميائي وتركيز المواد المتفاعلة على سبيل المثال ، التفاعل A B هو تفاعل من خطوة واحدة ، ويتم التعبير عن قانون معدله على النحو التالي : R = k [A] R يمثل سرعة التفاعل ، [A] تركيز المادة المتفاعلة ، بينما k هو ثابت سرعة التفاعل .
يتم التعبير عن معدل التفاعل من خطوة واحدة كمنتج لكمية ثابتة مضروبة في تركيز المادة المتفاعلة ، الرمز k هو قيمة عددية ثابتة تسمى ثابت معدل التفاعل. تتعلق هذه القيمة العددية بمعدل التفاعل لتركيز المواد المتفاعلة عند درجة حرارة معينة. ثابت المعدل هو قيمة محددة لكل تفاعل وله وحدات قياس مختلفة مثل L2 / mol2.s ، L / mol.s أو s-1 ، يجب تحديد قانون معدل التفاعل تجريبياً ، كما هو موضح في الشكل 13-3 .
شكل 3-13 عينات من خليط التفاعل يتم سحبها على فترات منتظمة لتحديد معدل التفاعل عند حدوثه ، ويتم حقن هذه العينات على الفور في جهاز الكروماتوغرافيا الذي يحدد مكوناتها ثم يفصلها عن بعضها البعض ، يوضح قانون المعدل أن معدل التفاعل يتناسب طرديًا مع التركيز المولى للمركب A ، لا يتغير ثابت معدل التفاعل k مع التركيز ، ولكنه يتغير مع درجة الحرارة تعني القيمة الكبيرة لـ k أن A يتفاعل بسرعة لتشكيل B .
قوانين معدل التفاعل من الدرجة الأولى :
من المعادلة الرياضية لمعدل التفاعل = k A من المفهوم أن التعبير A يعني A1 ، يُعرف الرقم الأعلى الذي يمثله أس المادة المتفاعلة A بترتيب التفاعل ، والذي يمكن تحديده من خلال معرفة تأثير التغيير في تركيز المادة المتفاعلة على معدل التفاعل على سبيل المثال ، يتم التعبير عن قانون معدل التفاعل لتحلل بيروكسيد الهيدروجين H O بواسطة المعادلة : R = k H2O2 .
تذكر أن معدل التفاعل يتحدد من البيانات التجريبية ، ونظرًا لأن ترتيب التفاعل يعتمد على معدل التفاعل ، فإنه يترتب على ذلك أن ترتيب التفاعل يتم تحديده أيضًا تجريبيًا أخيرًا ، نظرًا لأن ثابت المعدل k يصف معدل التفاعل ، يجب أيضًا تحديده تجريبيًا ، يوضح الشكل 3-14 كيف يتغير معدل تفاعل تحلل H2O2 الأولى مع تغير تركيز H2O2 .
قوانين معدل التفاعل للأوامر الأخرى :
الترتيب العام للتفاعل الكيميائي هو مجموع أوامر المواد المتفاعلة في تفاعل كيميائي ، من المعروف أن العديد من التفاعلات ، خاصة تلك التي تتضمن أكثر من مفاعل واحد ، ليست من الدرجة الأولى ، دعونا نفحص الشكل العام للتفاعل الكيميائي لمتفاعلين ، كما هو موضح في المعادلة التالية ، حيث يتم إعطاء أ وب في هذه المعادلة الكيميائية للمعاملات .
عروض باوربوينت درس قوانين سرعة التفاعل الكيميائي مادة الكيمياء 3 مقررات
يمكنك الحصول على التحضير الخاص لعروض باوربوينت درس قوانين سرعة التفاعل الكيميائي لمادة الكيمياء في المرحلة الثانوية كاملة وجميع ملحقاتها من خلال بريدك الإلكتروني بسعر 10 ريال فقط ، كل ما عليك فعله هو الاتصال بنا من خلال أرقام الواتساب الموضحة في أي لحظة سوف يرد عليك موظف المبيعات على مدار اليوم في أي وقت .



