ورق عمل درس الكتلة والمول مادة كيمياء 1 مقررات

ورق عمل درس الكتلة والمول مادة كيمياء 1 مقررات تعتبر مؤسسة التحاضير الحديثة من المؤسسات الرائدة في المجال التعليمي ، ويرجع ذلك لجودة التحاضير التي تقدمها للمعلمين خاصة في المواد العلمية مثل مادة كيمياء 1 مقررات التي تقدم لها تحاضير شاملة كل ما يخص المادة من أهداف وتوزيع وملفات أخرى مهمة .
ورق عمل درس الكتلة والمول مادة كيمياء 1 مقررات
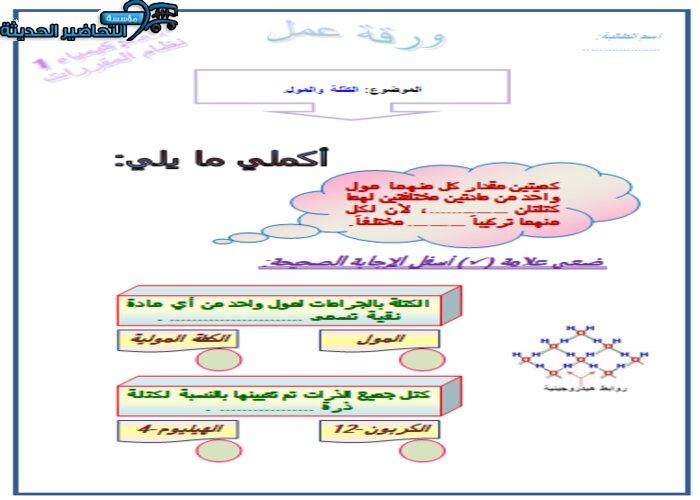
ما المقصود بالكتلة المولية ؟
الكتلة المولية لأي عنصر تساوي عدديًا كتلته الذرية ووحدته جم / مول ، وكما هو موضح في الجدول الدوري ، فإن كتلة ذرة الحديد هي 55.845 amu ، ومن ثم فإن الكتلة المولية للحديد هي 55.845 / مول لاحظ أنه بقياس 55.845 جم من الحديد ، سوف تحسب بشكل غير مباشر 6.02 × 10²³ ذرة ، يوضح الشكل 5-6 العلاقة بين الكتلة المولية والمول الواحد لعنصر ما .
تحضير درس الكتلة والمول مادة كيمياء 1 مقررات [varnumber]
مكونات مادة كيمياء 1 مقررات [varnumber]
طرق تحضير مادة كيمياء 1 مقررات [varnumber]
يمكنك الحصول على نسخة مجانية من تحضير مادة كيمياء 1 مقررات [varnumber]
يمكنك معرفة أسعار تحضير مادة كيمياء 1 مقررات[varnumber]
يمكنك تقديم طلبك للحصول على مادة كيمياء 1 مقررات[varnumber]
شرح درس الكتلة والمول مادة كيمياء 1 مقررات[varnumber]
تمهيد :
لن تتوقع أن تكون دزينة ليمون دزينة بيضات ؛ نظرًا لاختلاف البيض والليمون في الحجم والتركيب الكيميائي ، فليس من المستغرب أن يكون لهما كتل مختلفة ، كما هو موضح في الشكل 5-5 ، بالنسبة لذلك ، كميتين من مول واحد لكل من مادتين مختلفتين كتل مختلفة ، لأن لكل منهما تركيبة مختلفة .
مثال :
إذا وضعت مولا من الكربون ، على سبيل المثال ، وخلد من النحاس في مقياسين ، فسترى فرقًا في الكتلة ، كما ترى في كتل البيض والليمون ، يحدث هذا لأن كتلة ذرات الكربون تختلف عن كتلة ذرات النحاس ، وبالتالي فإن كتلة ذرات الكربون 6.02 × 10²³ لا تساوي كتلة ذرات النحاس 6.02 × 10²³ .
انظر إلى الشكل 5-5 :
شكل 5-5 كتل دستة ليمونة ضعف كتلة دستة بيضة. الفرق بين الكتلتين منطقي ؛ لأن الليمون يختلف عن البيض في التركيب والحجم ، شكل 5-6 مولات من الحديد ، تحتوي على عدد ذرات أفوجادرو ، ممثلة بكيس من الكتلة يساوي كتلتها الذرية بالجرام .
كيف ترتبط كتلة الذرة بكتلة الخلد في تلك الذرة ؟
تذكر ، يتم تعريف الخلد على أنه عدد ذرات الكربون 12 في 12 جرامًا منه. ثم الكتلة 1 مول من ذرات الكربون 12 هو 12 جم ، سواء كنت مهتما بذرة واحدة أو عدد ذرات أفوجادرو (1 مول) ، فإن كتل جميع الذرات يتم تخصيصها لكتلة ذرة الكربون 12 ، تسمى الكتلة بالجرام في مول واحد من أي مادة نقية الكتلة المولية .
كيفية تحويل المولات إلى الكتلة ؟
افترض أنك أثناء عملك في مختبر كيميائي ، تحتاج 3.00 مول من النحاس لتفاعل كيميائي ، كيف تقيس هذه الكمية ؟ ، من الصيغة : الكتلة (g) = عدد المولات (mol) × الكتلة المولية مقسومة على 1 مول ، للحصول على عدد المولات نضرب كلا الجانبين في مقلوب الكتلة المولية ، لذلك ، نجد أن تحويل الكتلة إلى مولات يتطلب استخدام مقلوب الكتلة المولية كعامل تحويل .
إذا نظرت إلى الجدول الدوري للعناصر ، فإن Cu-29 لها كتلة ذرية تبلغ 63.45 amu وأنت تعلم أن الكتلة المولية للعنصر (g / mol) تساوي الكتلة الذرية (معبرًا عنها في amu) ، ومن هنا الكتلة المولية للنحاس هي 63.546 جم / مول ، وباستخدام ذلك ، يمكنك تحويل 3.00 مول من النحاس إلى جرام من النحاس .
انظر إلى شكل رقم 5-7 :
كما هو موضح في الشكل 5-7 ، من الممكن قياس 3.00 مول من النحاس اللازم للتفاعل باستخدام ميزان لتخصيص 191 جم من النحاس ، ويتضمن التحويل العكسي (الكتلة إلى المولات) استخدام مقلوب الضرس الكتلة كعامل تحويل ، هل يمكنك أن تشرح لماذا ؟ ، لقياس 3.00 مول من النحاس ، ضع بطاقة على الميزان وصفرها ، ثم ضع 191 جم من النحاس .
إذا كنت مهتما بالتعرف على المحتوى التي تقدمه مؤسسة التحاضير الحديثة تفضل بزيارة موقع المؤسسة الرسمي .



